
Ayt Kimya Ve Elektrik Konu Anlatımı
Bu içerik, AYT kimya müfredatındaki elektrik konusunu ele alarak kimya ve elektrik arasındaki ilişkiyi, elektrokimyayı ve ilgili süreçleri detaylandırmaktadır. Elektroliz ve galvanik hücreler gibi temel kavramlarla birlikte, bu alandaki uygulamaların önemine vurgu yapılmaktadır.
Ayt Kimya Ve Elektrik Konu AnlatımıKimya, doğanın temel bileşenlerini ve bu bileşenlerin birbirleriyle etkileşimlerini inceleyen bir bilim dalıdır. Elektrik ise, atomların yük taşımayan parçacıkları olan elektronların hareketiyle ilgili bir fenomendir. Kimya ve elektrik arasındaki ilişki, özellikle elektro kimya alanında belirgin hale gelir. Bu yazıda, AYT kimya müfredatında önemli olan elektrik konusunu detaylı bir biçimde inceleyeceğiz. Kimya ve Elektrik İlişkisi Kimya ve elektrik arasındaki ilişki, özellikle kimyasal reaksiyonların enerji değişimleri ve elektron transferleri ile ilgilidir. Elektrokimyada, elektrik enerjisi kimyasal enerjiyi ve tam tersini dönüştürme süreçleri incelenir. Bu süreçler, pillerin ve elektroliz hücrelerinin çalışma prensiplerini anlamamızda hayati öneme sahiptir. Elektrokimya Nedir? Elektrokimya, kimyasal reaksiyonların elektrikle olan ilişkisini inceleyen bir bilim dalıdır. İki temel süreç vardır:
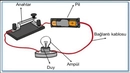
Elektroliz Süreci Elektroliz, bir çözeltinin veya eriyik haldeki bir bileşiğin elektrik akımı ile parçalanmasıdır. Bu işlem, genellikle bir elektrolit çözeltisi içerisinde gerçekleştirilir. Örneğin, suyun elektrolizinde su molekülleri, hidrojen ve oksijen gazlarına ayrılır. Bu süreç, suyun elektrik akımı ile ayrıştırılması yoluyla gerçekleştirilir. Galvanik Hücreler Galvanik hücreler, kimyasal enerjiyi elektrik enerjisine dönüştüren sistemlerdir. Bu hücrelerde, iki farklı metal elektrot ve bir elektrolit çözeltisi bulunur. Örneğin, çinko ve bakır metallerinin kullanıldığı bir hücrede, çinko oksitlenirken bakır indirgenir. Bu süreç, dış devre üzerinden elektrik akımının oluşmasına neden olur. Örnek Problemler 1. Bir galvanik hücrede çinko ve bakır metallerinin kullanılması durumunda, hangi metalin oksitlendiğini ve hangi metalin indirgeneceğini belirleyiniz. Cevap: Çinko oksitlenir, bakır indirgenir. 2. Suyun elektrolizi sırasında hangi gazlar oluşur? Cevap: Hidrojen ve oksijen gazları oluşur. Küçük Test Aşağıdaki soruları yanıtlayarak elektrokimya konusundaki bilginizi test edebilirsiniz.
Ekstra Bilgiler Elektrokimya, günlük yaşamda birçok uygulamaya sahiptir. Örneğin, piller ve aküler, elektrokimyasal süreçler sayesinde elektrik enerjisi depolayabilir ve serbest bırakabilir. Ayrıca, metal kaplama, elektrolizle gerçekleştirilen kimyasal bir işlemdir ve birçok endüstriyel uygulama için önem arz eder. Sonuç olarak, AYT kimya dersi için elektrik konusunun anlaşılması, hem teorik bilgi hem de pratik uygulamalar açısından önemlidir. Elektrokimya, öğrencilerin kimya ve fizik arasındaki bağlantıyı anlamalarına yardımcı olur ve çeşitli bilimsel ve teknik alanlarda kariyer fırsatlarını artırır. |
































Bu yazıda elektrokimyanın temel kavramları ve uygulamaları hakkında oldukça kapsamlı bir bilgi verilmiş. Özellikle elektroliz ve galvanik hücreler konusunun detaylı bir şekilde ele alınması, bu alandaki temel kavramların anlaşılması açısından çok faydalı. Bu bilgileri öğrenmek, günlük yaşamda karşılaştığımız pillerin ve akülerin nasıl çalıştığını anlamak için gerçekten önemli. Elektroliz sırasında suyun hidrojen ve oksijene ayrılması örneği çok öğretici. Bu tür basit ama etkili örneklerle konunun daha iyi pekiştirileceğini düşünüyorum. Ayrıca galvanik hücrelerde hangi metalin oksitlendiğini ve hangisinin indirgeneceğini anlamanın, elektrik akımının nasıl oluştuğunu kavramamıza yardımcı olacağını düşünüyorum. Galvanik hücre örneği de oldukça iyi bir uygulama olarak verilmiş. Ekstra bilgiler kısmında elektrokimyanın günlük yaşamda nasıl yer bulduğuna dair bilgiler verilmesi, bu konunun önemini daha da vurguluyor. Özellikle metal kaplama ve enerji depolama gibi uygulamalar, öğrencilerin elektrokimyasal süreçlerin gerçek hayattaki yansımalarını görmelerine yardımcı olur. Bu yazı, AYT kimya dersine hazırlananlar için gerçekten değerli bir kaynak oluşturuyor. Elektrokimya konusunu daha iyi anlamak için bu tür örnekleri ve uygulamaları incelemek oldukça faydalı olacaktır. Sizce elektrokimya ile ilgili başka hangi konulara da değinilmeliydi?
Elektrokimyanın Kapsamı
Uyguralp, elektrokimya alanında verdiğiniz bilgiler gerçekten çok değerli. Elektrokimyanın temel kavramlarını anlamak, günlük yaşamda karşılaştığımız birçok teknolojinin arka planını aydınlatıyor. Özellikle elektroliz ve galvanik hücreler gibi konular, bu bilim dalının pratikteki önemini gözler önüne seriyor.
Örneklerle Öğrenme
Suyun elektrolizi gibi basit ama öğretici örnekler, konunun daha iyi kavranmasına yardımcı oluyor. Bu tür örnekler, teorik bilgilerin pratiğe nasıl döküldüğünü gösteriyor. Ayrıca, galvanik hücrelerdeki metal oksidasyon ve indirgeme süreçlerinin anlaşılması, elektrik akımının nasıl oluştuğunu kavramamıza katkı sağlıyor.
Günlük Hayatla İlişkilendirme
Ekstra bilgiler kısmında, elektrokimyasal süreçlerin günlük yaşamda nerelerde kullanıldığını belirtmeniz de yazının değerini artırıyor. Metal kaplama ve enerji depolama gibi uygulamalar, öğrencilerin öğrenilen bilgilerin gerçek hayattaki yansımalarını görmelerine olanak tanıyor.
Ekstra Konular
Elektrokimya ile ilgili olarak, elektrokimyasal hücrelerin verimliliği, yeniden enerji üretimi ve çevre dostu uygulamalar gibi konulara da değinilmesi faydalı olabilir. Ayrıca, biyosensörler gibi yeni nesil uygulamalara dair bilgiler, öğrencilerin bu alandaki gelişmeleri takip etmelerine yardımcı olacaktır.
Sonuç olarak, elektrokimya konusunu daha derinlemesine incelemek, hem akademik anlamda hem de pratikte büyük yarar sağlayacaktır. Teşekkürler!